作者:安德鲁便士。Karalewitz博士。
日期: 2021年3月
免疫疗法代表了癌症治疗的最先进水平。通过利用免疫系统的特异性,现代免疫疗法可以设计成针对癌细胞类型,同时避免健康组织。诺华的Kymriah™和Kite/Gilead的Yescarta™是fda批准的细胞免疫疗法,分别用于治疗急性淋巴细胞白血病和弥漫性大B细胞淋巴瘤。
为了生产Kymriah™或Yescarta™,患者的T细胞被设计表达Chimeric一个ntigenR(1)随着最近抗CD19 CAR - T细胞治疗血癌的临床成功,人们正在设计具有增强活性和安全性的下一代CAR。
Labcorp临金博宝188网址床前肿瘤学(PCO)提供Chimeric一个ntigenR受体(CAR) T细胞生成。这项服务满足了对CAR - T细胞可靠来源的日益增长的需求,用于早期发现研究。赞助商可以使用预制的抗cd19 CAR - T细胞,或者客户可以使用定制CAR - T细胞生成服务提供慢病毒颗粒来表达他们选择的CAR。金博宝188网址对多种CAR候选药物的临床前评估将使发起人能够确定最活跃的CAR进行药物开发。CAR - T细胞生成服务建立在先前生成荧光素酶表达细胞系的经验基础上,并辅以内部处理和培养T细胞和CAR - T细胞的专业知识。CAR - T细胞生成服务为早期发现研究提供了足够数量的CAR - T细胞。
CAR - T细胞生成的工作流程由三个不同的技术阶段组成:CAR - T细胞生成,流式细胞术评估CAR - T细胞表达,以及体外培养在体外检测CAR - T细胞活性的杀伤试验。的在体外如果发起者已经有CAR - T细胞来源,并且有兴趣使用客户可获得的众多癌细胞系中的一种来测试CAR - T细胞功能,则可以将杀伤检测作为一项独立的服务。在这个模型聚焦中,CAR - T细胞生成服务使用抗cd19 CAR作为示例进行演示。
通过慢病毒转导产生抗cd19 CAR - T细胞
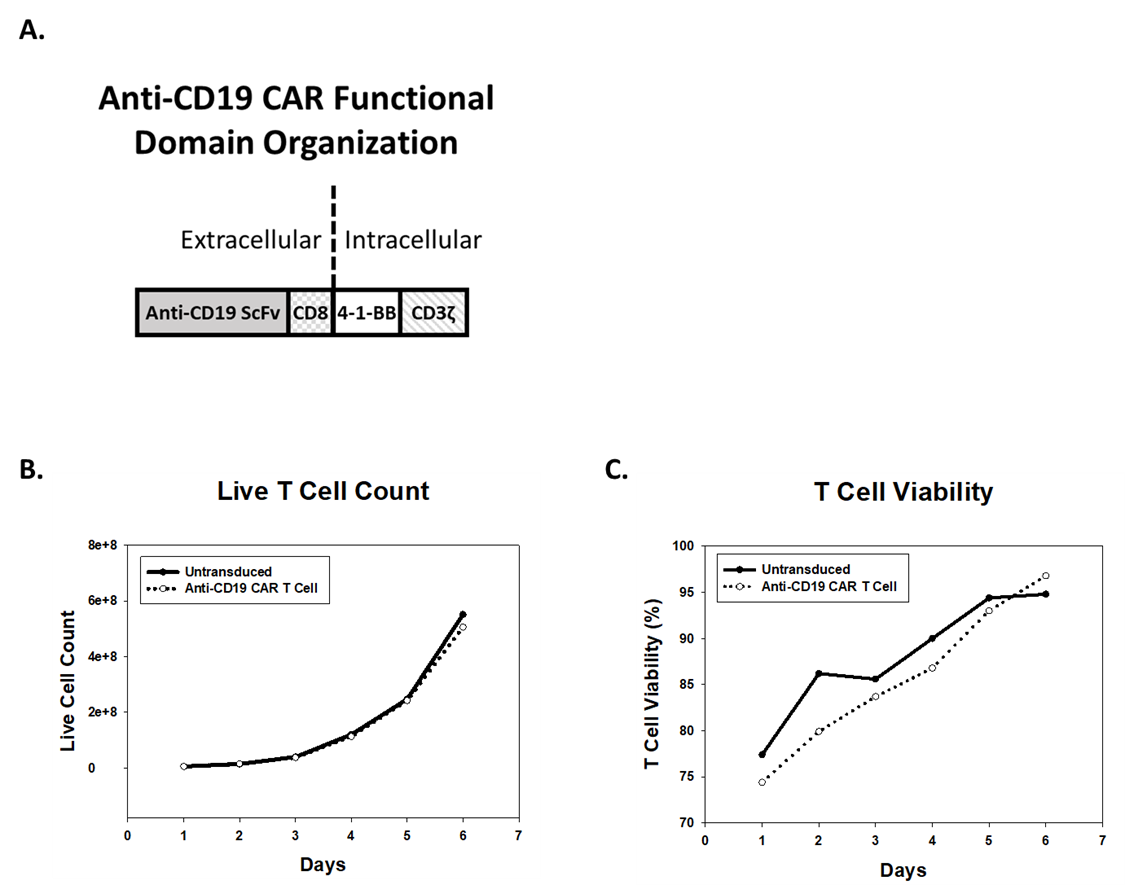
car是一种合理设计的蛋白质,由细胞外抗原受体与细胞内信号域融合而成。抗原受体通常基于单克隆抗体(mAb)的单链可变片段(ScFv)。细胞内信号域由T细胞特异性活性调节剂组成,如4-1-BB和TCR-ζ细胞质信号链(CD3ζ)。(图1)为了产生抗cd19的CAR - T细胞,一种慢病毒表达系统被用来将编码CAR结构的遗传物质传递到T细胞中。来自健康供体的人外周血单个核细胞(hpmcs)被慢病毒转导,在培养中扩增,随后冷冻保存以备将来使用。T细胞被病毒转导,或未转导的T细胞(UTD),增殖和转导后存活率大于90%(图1B及1C).
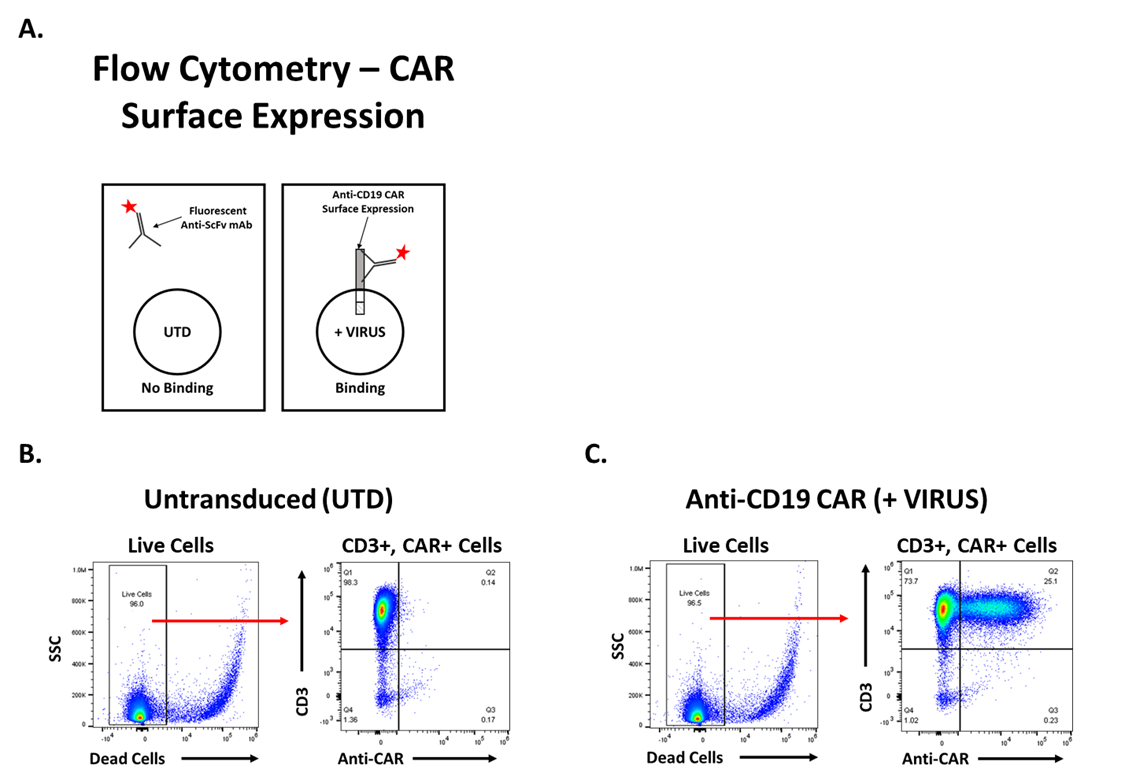
抗cd19 CAR表面表达的评估
抗cd19 CAR - T细胞的功能分析对于确定慢病毒转导是否成功是必要的。流式细胞术用于量化CAR+ T细胞的数量,并确定转导效率。使用特异性结合FMC63 ScFv的单抗检测抗cd19 CAR的表面表达(图2)。在门控排除双重结构和碎片后,鉴定活细胞,并确定CAR表达。未转导(UTD) T细胞96% CD3+和0.14% CD3+/CAR+(图2 b)。在T细胞被慢病毒处理后,大约25%的T细胞是CD3+/CAR+(图2)。双阳性T细胞(CD3+/CAR+)百分比的增加表明转导成功。基于活性染料排除,UTD和抗cd19 CAR - T细胞的活性均大于90%。
抗cd19 CAR - T细胞功能评估
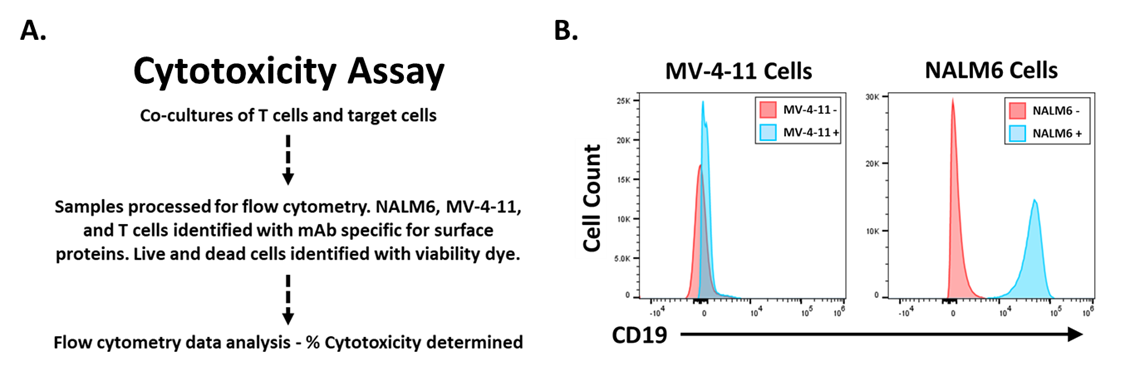
为了确定抗cd19 CAR - T细胞是否具有功能,进行了靶细胞杀伤试验(图3)。简单地说,目标细胞与UTD或抗cd19 CAR - T细胞共培养。第二天,用流式细胞术检测靶细胞活力。抗CD19 CAR - T细胞应该特异性杀伤表达CD19的靶细胞,而对不表达CD19的靶细胞没有作用。流式细胞术检测CD19在靶细胞表面的表达(图3 b)。NALM6细胞表达CD19, MV-4-11细胞不表达CD19(图3 b)。
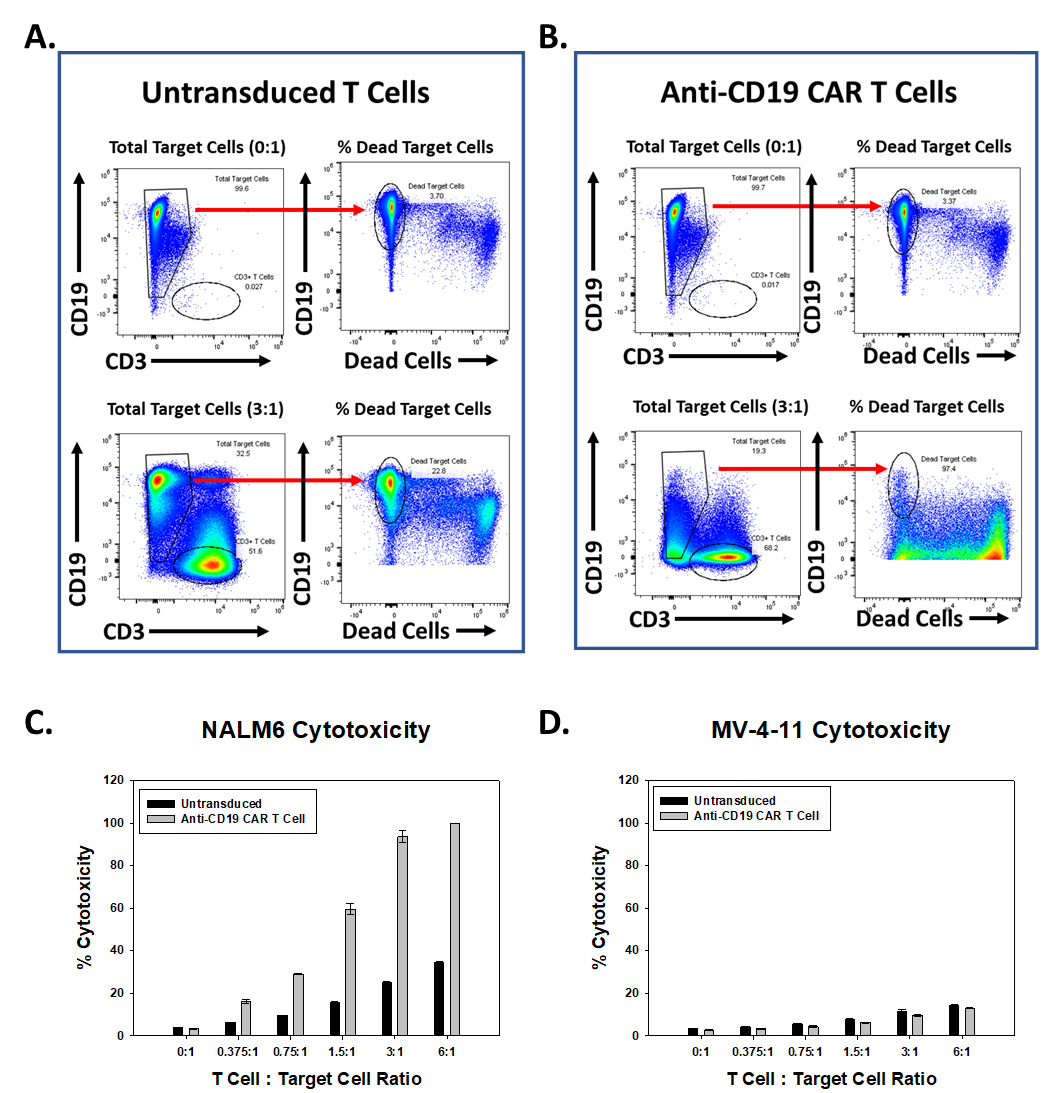
抗cd19 CAR - T细胞对NALM6细胞有细胞毒性吗(图4)。鉴定出CD19+ NALM6细胞和CD3+ T细胞群。对CD19+细胞总数进行门控后,测定死亡CD19+细胞的百分比。活细胞CD19+/活性染料阴性。单独培养的靶细胞存活率为96%。反向门表示靶细胞死亡百分比(3.7%)(图1).与UTD T细胞孵育的NALM6细胞相比,在抗cd19 CAR - T细胞培养的孔中观察到更大比例的NALM6细胞死亡(图4A、B、C)。UTD和抗cd19 CAR - T细胞对MV-4-11细胞的细胞毒性百分比相同(图4 d)。结果表明,抗cd19 CAR - T细胞对表达cd19的靶细胞具有特异性活性,验证了CAR - T细胞生成服务的成功
总结
从健康的人体pbmc开始,Labcorp的CAR - T生成服务生产足够数量的CAR+ T细胞在体外而且在活的有机体内鉴定。这里描述的CAR - T细胞生成服务生产的最终产品是>95% CD3+, >90%存活,对表达cd19的人淋巴母细胞白血病细胞具有特异性细胞毒性。T细胞转导方案基于现有技术,也适用于其他CAR结构,允许Labcorp为我们的客户提供定制的CAR - T生成服务(2)。生成用于临床前研究的CAR - T细胞将促进我们客户使用组合或新型CAR - T疗法的早期发现项目。金博宝188网址
参考文献
1) June CH, O 'Connor RS, Kawalekar OU, Ghassemi S, Milone MC. CAR - T细胞免疫治疗人类癌症。科学。2014;359 (6382): 1361 - 1365
2) Quintás-Cardama A, Yeh RK, Hollyman D, Stefanski J, Taylor C, Nikhamin Y, Imperato G, Sadelain M, Rivière I, Brentjens RJ。多因素优化γ -逆转录病毒基因转入人T淋巴细胞临床应用。哈姆·吉恩·瑟尔,2007;18日(12):1253 - 60
连接
让我们开始对话吧
188 bet 服务中心

